Historique de Marseille
| liens |
le 18/08/17
| ��L’actualité du LAM | ��Le cours à l’Observatoire Historique de Marseille |
| �� Mis à jour le 18/08/17 |
||||
| �� Fiches : réactions nucléaires | |||||||
En cours de rédaction…
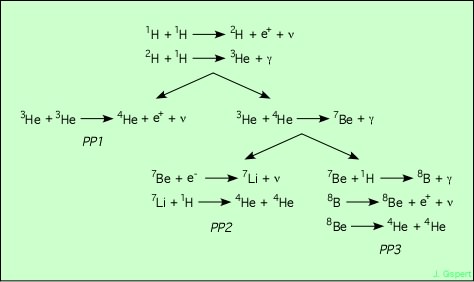
Ces réactions se produisent à une température de 15 millions de degrés (atteinte dans le coeur du soleil).
Toutes ces réactions ne se produisent pas à la même vitesse ; remarquons tout d’abord que dans la première, l’atome produit, noté 2H, est un atome de Deutérium (encore appellé hydrogène lourd et alors noté D ; c’est lui qui, lié à l’oxygène, donne la molécule d’eau lourde D2O). Or cet atome ne comprend pas deux protons, mais un proton et un neutron. Donc, dans la bataille (de la réaction, pas de l’eau lourde !), un proton (l’un des noyaux d’hydrogène) s’est forcément transformé en neutron. Nous sommes en train d’étudier des réactions nucléaires, basées sur l’interaction forte, mais cette transformation proton-neutron fait intervenir l’interaction faible (désintégration béta). Or les réactions dues à l’interaction faible sont considérablement plus lentes que celles dues à l’interaction forte. C’est donc elle qui va ralentir énormément le processus de transformation de l’hydrogène en hélium. Heureusement, car sans cela, il y a longtemps que le Soleil aurait fini de briller !
Pour être complet, il faudrait mentionner deux variantes du cycle proton-proton. Celle donnée ci-dessus se nomme alors PPI, et les deux autres PPII et PPIII. Elles font intervenir le lithium et le berylium, qui sont des noyaux très fragile, qui en fait se brisent en général avant de pouvoir intervenir dans une autre réaction. Pour cette raison, l’efficacité de ces variantes est beaucoup plus faible que celle du cycle principal.
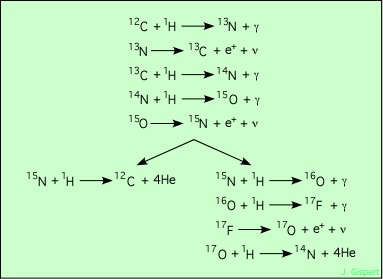
Le cycle du carbone a deux variantes ; la première restitue le carbone utilisé dans la première réaction, alors que la seconde produit de l’azote dans la dernière réaction. En fait, l’azote produit peut intervenir dans la quatrième réaction de la première forme, et donc redonner du carbone au bout du compte. Dans une telle réaction, le carbone est appellé catalyseur, puisque finalement l’atome de carbone utilisé est restitué. Tout se passe donc comme s’il avait facilité la réaction sans intervenir lui-même (sa présence est bien sûr obligatoire ; sans lui, les réactions n’ont pas lieu).
Le cycle du carbone se produit à température de 20 millions de degrés au moins. C’est pourquoi le moteur du soleil est alimenté essentiellement par le cycle proton-proton. Par contre, dans des étoiles plus massives, la température centrale est plus élevée, et le cycle de carbone devient prédominant.
Le bilan global de toutes ces réactions peut s’écrire : 4 1H → 4He ; en effet, tout le reste est restitué à la fin de la réaction. Seul l’hydrogène a été transformé. C’est pour cette raison qu’on dit que les étoiles transforment l’hydrogène en hélium.
La fusion de l’hélium donne essentiellement deux produits, le carbone et l’oxygène. Elle commence par la réaction triple alpha, ainsi nommée parce qu’elle implique 3 particules alpha (noyaux d’hélium) dans un temps extrêmement bref.
| Rencontre de deux alpha | 4He + 4He → 8Be + γ |
| puis presque simultanément | 8Be + 4He → 12C + γ |
Ce processus a été proposé dans les années 50 par Edwin Salpeter. Ce sont les réactions de fusion de l’hélium, qui se produisent lorsque l’hydrogène est épuisé. Température nécessaire : 100 millions de degrés ; densité minimum : 100 kg/cm3.
4He + 12C → 16O + γ
12C + 12C → 20Ne + 4He16O + 16O → 28Si + 4He
12C + 16O → 24Mg+ 4He
28Si + γ → 24Mg+ 4He
28Si + 4He → 32S + γ
32S + 4He → 36Ar + γ etc.
| Elément | Période |
|---|---|
| Ca 41 | 100.000 ans |
| Sn 126 | 200.000 ans |
| Cl 36 | 300.000 ans |
| Al 26 | 716.000 ans |
| Se 79 | 1,1 millions d’années |
| Be 10 | 1,5 millions d’années |
| I1 29 | 15,7 millions d’années |
| K 40 | 1,25 milliards d’années |
| U 238 | 4,5 milliards d’années |
| Th 232 | 14 milliards d’années |
Le césium Cs 137 (période 30,15 jours), l’iode I 131 (période 8,02 jours), le xénon Xe 133 (période 5,3 jours), ne sont pas présents dans notre environnement naturel. Ils ont été rejetés dans l’atmosphère par les accidents nucléaires de Tchernobyl, et de Fukushima. Ils résultent des réactions de fission, et sont produits à faible taux par la fission naturelle (uranium en particulier). Mais leur courte période les élimine très rapidement.
Muon
Le muon est un électron lourd, qui présente les mêmes caractéristiques quantiques que l’électron, à l’exception de sa masse. Celle-ci est de 207 fois celle de l’électron. Mais du fait de cette grande masse, le muon est instable et se désintègre en un électron, un neutrino muonique et un antineutrino électronique. La durée de vie du muon est de 2,2 microsecondes.
A la vitesse de la lumière, il peut donc parcourir x = c t = 3 105 km s-1 x 2,2 10-6 s = 6,6 10-1 km = 660 m.
Or ils sont produits en altitude dans l’atmosphère, et par conséquent ne devraient pas être observés au sol. Mais la durée de vie indiquée est celle ressentie par le muon, et non celle vue par l’observateur au sol. Pour celui-ci, la durée de vie est augmentée selon la formule relativiste :
tobs = t / sqrt(1 - v2 / c2)
Pour le muon, v = 0,995 c
donc v2 / c2 = 0,9952 c2 / c2 = 0,990025
tobs = t / sqrt(1 - 0,990025) = t / 9,9874921777 10-2
tobs = 10 t
La durée de vie apparente étant donc 10 fois supérieure à la durée de vie réelle, le muon parcours une distance 10 fois supérieure, donc 6,6 km. Ceci permet à de nombreux muons de parvenir jusqu’au sol.
---=OO=---